ATOMATOMLA İLGİLİ DÜŞÜNCELER
Atom, bir maddenin özelliklerini taşıyan ve kimyasal yöntemlerle daha fazla bölünemeyen en küçük parçacığıdır. Atom, duyu organlarımızla fark edilemeyecek kadar küçük olduğu için atomun yapısını kavramak, ancak deneysel gözlemlere dayalı akılcı tahminlerle mümkün olabilir. Deneysel gözlemlere dayalı, akılcı ve açıklayıcı şekillere model denir. Maddenin atom adı verilen küçük taneciklerden oluştuğu sonucuna götüren ilk deneysel çalışmalar 18. yüzyıl sonlarında Antoine Lavoisier ve Joseph Proust tarafından yapılmıştır. 9. sınıfta da öğrendiğiniz gibi Lavoisier, maddelerin gerçekleştirdiği yanma olayı ile ilgili uyguladığı deneyler ve ölçümlerle Kütlenin Korunumu Yasası'nı oluşturmuştur. Kütlenin Korunumu Yasası: Bir kimyasal tepkimede kütle yoktan var edilemez, var olan yok edilemez. Lavoisier' in deneysel çalışmalarını izleyen Proust, uyguladığı deneyler sonrasında Sabit Oranlar Yasası olarak bildiğimiz yasayı ileri sürmüştür. Sabit Oranlar Yasası: Bir bileşiği oluşturan atomların kütleleri arasında basit ve tam sayılarla ifade edilen sabit bir oran vardır.
Dalton Atom Modeli (1808)

Dalton kendi adıyla bilinen atom modelini, sabit oranlar kanunundan yararlanarak ortaya koymuştur. Bu kanuna göre elementler birbirleriyle belirli miktarlar ya da kısımlar halinde birleşir. Dalton'un atom teorisi şöyledir:
1870-William Crocks Elektronlar İçin İlk Kanıt---> Katot Işınları
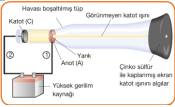
Elektronların varlığına dair ilk kanıt William Crooks ( William Crookes )tarafından ortaya konuldu. Crooks oluşturduğu tüpte elektrotlar arasına yüksek gerilim uygulayarak tüpün çeperlerini sarı-yeşil renkte ışınların aydınlattığını gözledi. Tüpün ortasına yerleştirdiği bir cismin gölgesinin tüpün sonunda görülmesinin sebebini tüpün içinde oluşan ışınların varlığından kaynaklandığını belirtti. Bu ışınlar katot ışınları olarak bilinir. Crocksun oluşturduğu bu tüpe katot ışın tüpü denir Katot ışınları, tüpün içine konulan gazın ve elektrotların yapıldığı cismin özelliklerine bağlı değildir. NOT: Bu keşiften sonra Julius Plucker, katot tüpünde mıknatısla katot ışınlarının yön değiştirmelerini ve davranışlarını ilk izleyen bilim adamı olmuştur.
1873-James Maxwellà Işık bir elektromanyetik dalgadır.
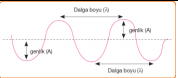
Gözümüz yayınlanan bu ışınların sadece
dalga boyu (λ ) 7.10 5 cm olan kırmızı ışık ile
4,5.10-5 cm olan mor ışık arasındaki kısmı görür.
Daha kısa dalga boylu ışımaları duyu organlarımızla algılayamayız.
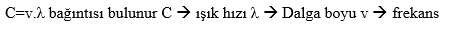
1874-Stoney àElektrik taneciklerden oluşur, Elektronun keşfi
Elektriğin taneciklerden ibaret olduğunu ve bu taneciklerin atomun yapısındada bulunduğunu söylemiştir. Gaz boşalma tüplerinde(-)yüklü tanecikler keşfedilmiştir. 1891 yılında bunları elektron olarak adlandırmıştır.
1886-Goldstein --->Pozitif Işınların Keşfi-Protonun keşfi
Gaz boşalması tüplerinde negatif parçacıklar gözlendiğine göre, maddenin nötral yapısı nedeniyle pozitif tanecikli yapılarında bulunduğu fikri geliştirmiştir. Gaz boşalma tüplerinde yapılan deneyler sonucunda pozitif ışınları ilk olarak Goldstein gözlemiştir.
1893-Wilhelm Wienà Siyah Cisim Işıması
Üzerine gelen bütün ışınları soğuran maddelere siyah cisim denir. Siyah cisimler farklı sıcaklıklarda farklı renkte ışımalar yaparlar. Bu dalga boyuyla ilişkilidir ve klasik fizik bunu açıklayamıyordu. Daha sonra plank kuantum fikrini ortaya atarak dalga kuramındaki bir eksiği gidermiştir.
1897-Thomson Atom Modeli
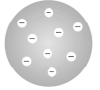
Maddenin yapısında proton ve elektronların varlığının kanıtlanması, proton kütlesinin elektron kütlesinden çok büyük olması, J.J. Thomson'ın Dalton atom modelinden daha gelişmiş bir model ortaya atmasına neden oldu. Thomson'a göre; Atom küre şeklindedir ve yaklaşık çapı 10–10 metredir.
(+) yüklerin (proton) ve (–) yüklerin (elektron) atomda homojen dağıldığı iddiası yanlıştır. Ayrıca bu modelde nötrondan ve atom çekirdeğinden bahsedilmemesi modelin eksik bir tarafıdır.