ALKİNLER (ASETİLENLER)
Genel formülleri CnH2n-2 şeklinde olan ve yapılarında en az bir üçlü bağ içeren bileşiklerdir.
Bu bileşiklere, moleküllerindeki üçlü bağ içermeleri ve sadece karbon ve hidrojenden oluşmalarından ötürü doymamış hidrokarbon da denir. Alkinlerin yapısında bulunan üçlü bağdan dolayı en az iki tane pi bağı vardır. Alkinlerin ilk üyesi önemli bir organik bileşik olan ve iki karbonlu etin (asetilen) olarak bilinen C2H2 bileşiğidir. Bu nedenle alkinlere asetilen sınıfı bileşikler de denir. Asetilen doğrusal bir geometriye sahiptir ve bağ açısı 180o ‘dir. Asetilenin bir hidrojen eksik hâline etinil denir.
Alkinlerin Adlandırılması
1. Üçlü bağın içinde bulunduğu en uzun zincir seçilir.
2. Ana zincire numara verme işlemi üçlü bağa göre yapılır. Üçlü bağ hangi uca yakınsa numara verme işlemine o uçtan başlanır.
3. Üçlü bağ her iki uca eşit mesafede ise alkanlardaki kurallar sırası ile uygulanır. Önce dallanma önceliğine, sonra alfabetik önceliğe bakılır.
4. Bileşikteki yan grupları adlandırma işlemi alkanlardaki kurallara göre yapılır. Yan gruplar yazıldıktan sonra üçlü bağın bulunduğu karbonlardan numarası küçük olanın numarası yazılır ve ana zincirin karşılığı olan alkanın sonundaki -an eki yerine -in eki getirilerek adlandırma yapılır.
5. 2 ve 3 karbonlu alkinlerde üçlü bağın yerini belirtmeye gerek yoktur.
6. Birden fazla üçlü bağ varsa her bir üçlü bağın yeri ayrı ayrı belirtilir ve -in ekinden önce üçlü bağların sayısı iki ise -diin, üç ise -triin ekleriyle belirtilir.
Alkinlerin Özellikleri
Alkinler de alkenler ve alkanlar gibi apolar bileşiklerdir. Yapılarında bulunan üçlü bağlardan iki tanesi pi bağıdır. Bu pi bağları açılarak katılma tepkimesi gerçekleştirir. Yapısındaki üçlü bağ 1 ve 2 numaralı karbonlar arasında olan alkinlere uç alkin, ana zincirdeki diğer karbonlar arasında olan alkinlere ise iç alkin denir.
Asetilenin Kimyasal Reaksiyonları
1. Katılma Reaksiyonları
Asetilen, yapısında pi bağı bulundurduğundan katılma tepkimesi verir.
a) H2 Katılması: Asetilene palladyum (Pd) katalizörlüğünde 1 mol H2 katılırsa alken, platin (Pt) katalizörlüğünde 2 mol H2 katılırsa alkan elde edilir.
b) Halojen Katılması: Asetilen, halojenlerle katılma tepkimesi verir ve bromlu suyun kırmızı rengini giderir. Asetilene 1 mol Br2 katılırsa 1,2-dibromo eten, 2 mol Br2 katılırsa 1,1,2,2-tetrabromo etan elde edilir.
c) Halojen Asidi Katılması: Asetilene 1 mol HCl katılırsa kloroeten (vinil klorür) elde edilir.
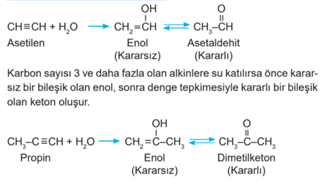
d) Su Katılması: Asetilen, su ile katılma tepkimesi vererek önce kararsız bir bileşik olan enol, sonra denge tepkimesiyle kararlı bir bileşik olan asetaldehit oluşturur.
2. Polimerleşme Reaksiyonu
a) Üç tane asetilen bileşiğinin 600 oC sıcaklıkta bir araya gelmesiyle (trimerleşme) benzen bileşiği elde edilir.
b) Asetilene HCl katılması ile oluşan vinil klorür polimerleşerek günümüz inşaat sektöründe çok önemli bir yere sahip olan polivinil klorür (PVC) bileşiğini oluşturur.
3. Yer Değiştirme Reaksiyonları
Asetilen, amonyaklı AgNO3 çözeltisiyle tepkime vererek beyaz çökelek oluşturur. Amonyaklı AgNO3 (Tollens ayıracı) önce [Ag(NH3)2]+ kompleks iyonunu, sonra asetilenle tepkimeye girerek suda çözünmeyen beyaz renkli çökelek oluşturur.
AROMATİK HİDROKARBONLAR(ARENLER)
Baharatların birçoğunun kendine has ve güzel kokuları, yapılarında bulunan altı karbonlu halkalı yapıda olan benzen molekülünü içeren kimyasal maddelerden kaynaklanmaktadır.
Kendine has kokuları olan bu bileşiklere güzel kokulu anlamına gelen aromatik bileşik (aren) denir.
Benzen: Aromatik hidrokarbonların ilk üyesi 6 karbonlu benzendir.
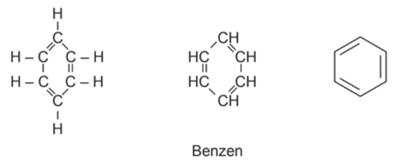
Benzenin yapısında bulunan karbon atomları arasında 3 tane tekli, 3 tane ikili bağ vardır. Benzendeki pi bağları birbirleriyle sürekli yer değiştirir ve çok kararlı bir yapı oluşturur. Bu duruma rezonans denir. Benzenin rezonans yapısından dolayı karbon atomları arasında bulunan bütün bağlar özdeştir.
Benzen kararlı yapısından dolayı doymamış bir hidrokarbon olmasına rağmen katılma reaksiyonu vermez. Aromatik bileşiklerin bir hidrojen eksik hâline aril, benzen halkasının bir hidrojen eksik hâline fenil denir.
Naftalin: İki benzen halkasının kaynaşmasıyla oluşan, formülü C10H8 olan aromatik bileşiğe denir. Oda şartlarında beyaz, kristal yapılı bir katı olan naftalin, kolayca süblimleşir. Kendine özgü keskin bir kokusu vardır. Bu keskin koku sayesinde haşereleri uzaklaştırdığından kumaş ve yünlerin korunması için günlük hayatta kullanılır.
Anilin: Benzen halkasına amino (–NH2) grubu bağlanmasıyla oluşan aromatik bileşiğe denir. Renksiz, yağ görünümünde, özel kokulu, zehirli, 182 oC’ de kaynayan bazik bir sıvı olan anilin, boya sanayisinde çıkış maddesi olarak kullanılan önemli bir bileşiktir. Anilin ayrıca vernik, mürekkep, kauçuk ve lastik üretiminde kullanılır.
Toluen: Benzen halkasına metil (–CH3) grubu bağlanmasıyla oluşan aromatik bileşiğe denir. Renksiz, kendine has bir kokusu olan, kolay tutuşabilen bir sıvıdır. Plastik, ilaç, parfüm, boya ve patlayıcı bir madde olan TNT (trinitrotoluen) üretiminde kullanılır.
Fenol: Benzen halkasına hidroksil (–OH) grubu bağlanmasıyla oluşan aromatik bileşiğe denir. Kendine has bir kokusu olan fenol, oda şartlarında sıvı hâldedir. Zayıf asit özelliği gösterir. Çok geniş bir kullanım alanına sahiptir. Mikrop öldürücü özelliğinden dolayı tıpta uzunca bir süre antiseptik olarak kullanılmıştır.
FONKSİYONEL GRUPLAR
Bu bileşiklerden bir tane hidrojen atomunun ayrılmasıyla radikal gruplar oluşur ve R– ile gösterilir. Radikal gruplara fonksiyonel grup ya da grupların bağlanmasıyla farklı organik bileşikler meydana gelir. Radikal gruplara bağlanan bu farklı gruplara fonksiyonel grup denir. Fonksiyonel grup, bulunduğu organik bileşiğe belirli özellikler kazandıran ve tepkimelerinde etkin rol oynayan atom ya da atom gruplarıdır.
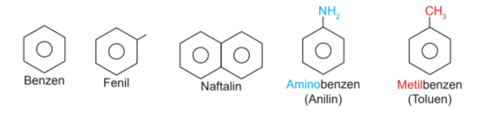
Bazı fonksiyonel gruplar şunlardır: