ISI VE SICAKLIK
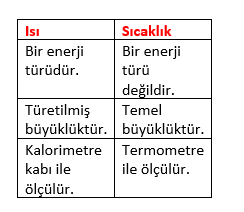
Sıcaklık: Bir maddenin taneciklerinin ortalama kinetik enerjisinin göstergesidir. Sembolü T ile gösterilir.
Birimi SI birim sisteminde Kelvin(K)dir.
Isı: Sıcaklığı farklı iki maddenin sıcaklığı yüksek olandan sıcaklığı az olana transfer ettiği enerjiye denir. Sembolü Q ile gösterilir.
Birimi SI birim sisteminde joule(j)dür.
1 cal = 4,18 joule
İç Enerji: Maddenin moleküllerinin titreşiminden dolayı sahip olduğu kinetik enerji ile moleküllerin bağlarından dolayı sahip olduğu potansiyel enerjinin toplamına denir.
bağlıdır.
ISI İLETİM YOLLARI
Isının tanecikler olmadan ışınlar sayesinde yayılmasına ışıma yoluyla ısı iletimi denir. Işımayla ısının yayılması boşlukta ve saydam ortamlarda gerçekleşir.
Isının hava veya sıvı akımı ile yani taneciklerin yer değiştirmesi ile yayılmasına ısının konveksiyon yolu ile yayılması denir. Sıvı ve gazlarda görülen ısının iletilme yoludur.
Isının katılarda iletim şeklidir. Maddenin taneciklerinin birbirine çarparak ısı enerjisinin aktarılmasına iletim yoluyla ısının yayılması denir.
Termometreler
Yüksek sıcaklıklar, metal termometreler ile ölçülür. Metallerin sıcaklık değişimiyle genleşme özelliğinden faydalanılır.
Hassas sıcaklıklar, gazlı termometreler ile ölçülür. Gazların sıcaklığa bağlı olarak basıncının değişmesi özelliğinden faydalanılır.
Günlük sıcaklıklar, sıvılı termometreler ile ölçülür. Sıvıların sıcaklık değişimiyle genleşme özelliğinden faydalanılır.
Sıvılı termometrelerin hassas ölçüm yapabilmesi için,

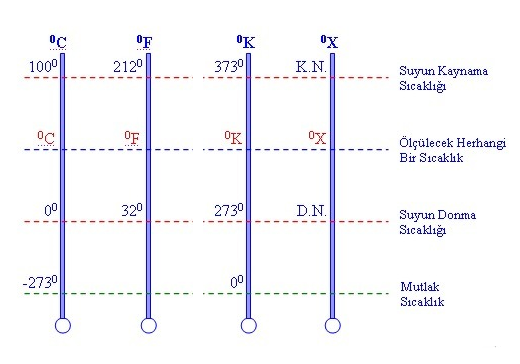
Sıcaklık Ölçekleri
Suyun kaynama ve donma noktasına göre farklı ölçekler içeren termometreler oluşturulmuştur.
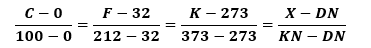
Özısı: Bir maddenin bir gramının sıcaklığını 1°C değiştirmek için gerekli ısı miktarıdır.
Isı sığası: Bir maddenin sıcaklığı 1°C değiştirmek için gerekli ısı miktarıdır.
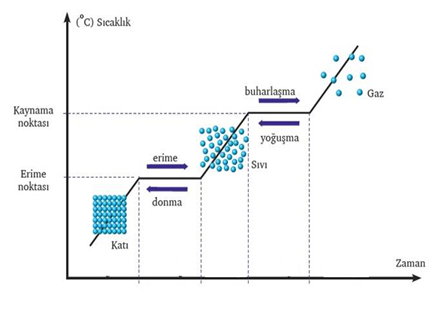
HAL DEĞİŞİMİ
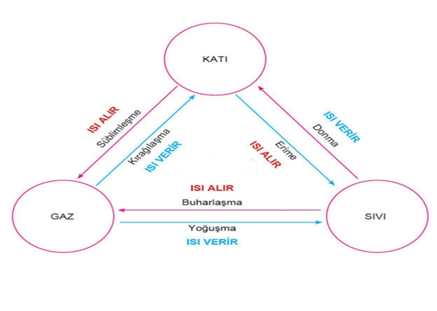
Hal değişim ısısı: Bir maddenin bir gramının hal değiştirmesi için gerekli ısı miktarıdır.
LERİME = LDONMA
LYOĞUŞMA = LKAYNAMA Hal değişimi durumunda madde heterojen (katı+sıvı ya da sıvı+gaz) halde bulunur.
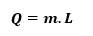
Hal değişim sıcaklığı: Bir maddenin hal değişimine başladığı sıcaklığa denir.
Erime noktası= Donma noktası Kaynama noktası = Yoğuşma noktası Örneğin; su 0°C de donar, buz 0°C de erir.
ÖNEMLİ BİLGİLER

!!! Buharlaşan bir sıvı yüzeyinden ısı alır. Terleyen insanların üşümesinin nedeni budur.
Isıl Denge Dış ortamdan ısıca yalıtılmış cisimler arasında sıcaklık farkından dolayı ısı alışverişi gerçekleşir. Isı akış yönü; sıcaklığı fazla olandan sıcaklığı az olana doğrudur. Isı alışverişi ısıl sağlandığında maddelerin sıcaklığı eşitlenir.
Bu sıcaklık;
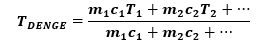
İle hesaplanır. İki maddenin transfer ettiği ısı birbirine eşittir.
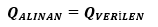
!!! Son sıcaklık ısı sığası büyük olan maddenin ilk sıcaklığına yakın olur.
Hal değişim grafiği